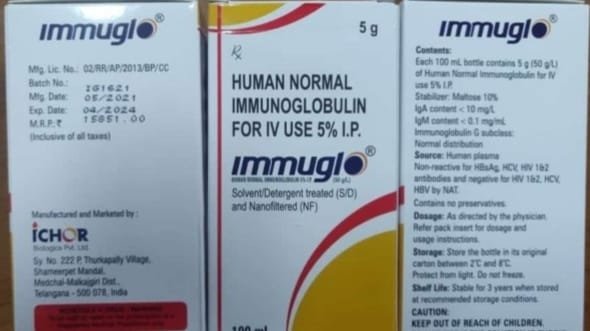
Tras varias denuncias, la Agencia Estatal de Medicamentos y Tecnologías en Salud (Agemed) instruyó ayer miércoles a la empresa importadora del medicamento Immuglo al 5% retirar todas sus unidades distribuidas de Cochabamba en un plazo de 72 horas, luego de constatarse que el fármaco ocasionó efectos adversos en los pacientes a los que fue suministrado.
“La resolución emitida por la Agemed es la cancelación del registro sanitario. Ya está notificada la empresa y tiene 72 horas para retirar, no solamente un lote, todos los lotes que habrían arribado al país. Setenta y dos horas es el plazo para que retire el lote de Cochabamba y del resto del país hasta tres meses, por el tema de logística”, precisó el director de la Agemed, Yuri Quisbert, según informó hoy el diario Opinión.
NIÑOS AFECTADOS
Andrea Antezana, una de las madres afectadas, denunció que 12 niños y niñas recibieron el medicamento, desde el 23 de diciembre de 2022.
Precisó que todos presentaron efectos adversos marcados por convulsiones, fiebre, náuseas, escalofríos, vómitos y dolores abdominales, entre algunos. Uno de los menores que presenta fibrosis renal manifestó insuficiencia renal y un bebé ingresó a Terapia Intensiva, por una infección derivada de su consumo.
“Hemos tenido presencia de quemaduras, hemos tenido la presencia también de convulsiones severas que han sido tan graves que incluso uno de nuestros niños se ha olvidado de masticar, y ha empezado a microaspirarse y le han puesto un botón gástrico a ese niño. Actualmente, se alimenta por botón gástrico. El otro pacientito está con insuficiencia renal”, relató Antezana.
MEDICAMENTO
El medicamento (inmunoglobina), que actuaba en calidad de “defensas artificiales”, era administrado cada 21 días. Antezana informó que con miras a evitar los efectos adversos, el personal médico procedió a los cambios de lotes del producto, incluso modificó el tiempo de su aplicación y fue administrando con otros medicamentos. Sin embargo, nada detuvo los efectos.
Ante ello, los padres de familia acudieron al Servicio Departamental de Salud (SEDES), Defensoría, Agemed e incluso al Ministerio de Salud. Lamentablemente, nadie actuó a tiempo y, por el contrario, les indicaron que “no existían pruebas suficientes para que este medicamento se retire”.
AGEMED AUTORIZÓ FÁRMACO
El director de la Agemed informó que la institución nacional autorizó el producto con su respectivo registro sanitario, en agosto de 2022. Sin embargo, es preciso resaltar que Brasil emitió una alerta de seguridad por efectos adversos de este medicamento en julio de 2022 y lo prohibió en diciembre.
Quisbert también precisó que la Agemed recibió la denuncia en enero de 2023, por parte de la Comisión de Farmacovigilancia del Hospital del Niño de Cochabamba, la cual dio cuenta de una posible reacción adversa.
Tras ello, la Agemed activó los mecanismos de control y vigilancia para conformar las denuncias. La vigilancia fue realizada en Santa Cruz, Cochabamba y La Paz, además del Hospital del Niño y en la empresa importadora del producto, donde se halló cinco lotes, los cuales fueron precintados, mientras duró la investigación.
Tras concluir la investigación, la empresa tiene un plazo de tres días para retirar todos sus lotes de Cochabamba y tres meses, del país.
La empresa importadora también deberá proceder a la destrucción de todos los medicamentos retirados. La Unidad de Vigilancia y Control de la Agemed hará seguimiento de ello.
SEDES
Hoy, desde el SEDES, que tuvo conocimiento del caso en abril, la responsable de Farmacias del Sedes, Dulcenia Claure, informó que se desconoce la cantidad de pacientes que recibieron dosis del fármaco; sin embargo, están siendo tratados.
En la entidad sanitaria indicaron que este medicamento incorporado al Seguro Universal de Salud (SUS) es “único” en su tipo, razón por la cual se deberá sumar otro.
Opinión